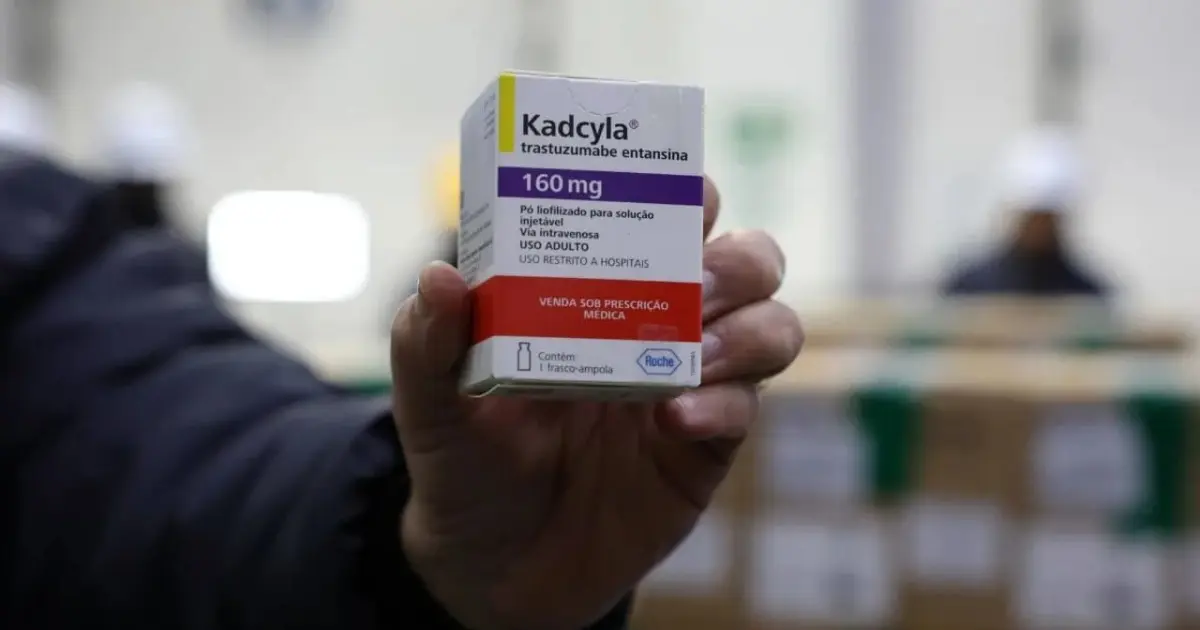
Bahia receberá mais de 700 frascos de medicamento inédito para tratar câncer de mama pelo o SUS
A Bahia vai receber 724 frascos do Trastuzumabe Entansina, medicamento de última geração incorporado recentemente ao Sistema Único de Saúde (SUS) para o tratamento do câncer de mama HER2-positivo, uma das formas mais agressivas da doença. A entrega está prevista para esta quinta-feira (23).
O fármaco faz parte do primeiro lote distribuído pelo Ministério da Saúde, que recebeu 11.978 unidades — sendo 6.206 frascos de 100 mg e 5.772 de 160 mg. A remessa chegou ao Brasil em 13 de outubro, pelo aeroporto de Guarulhos (SP).
De acordo com o ministério, a Secretaria Estadual de Saúde da Bahia (Sesab) ficará responsável pela distribuição do medicamento, seguindo os protocolos clínicos vigentes. O Trastuzumabe Entansina será destinado a pacientes que ainda apresentam sinais da doença após a quimioterapia inicial, geralmente em casos de câncer de mama HER2-positivo em estágio III.
O medicamento promete ampliar significativamente as chances de controle da doença e melhorar a qualidade de vida das pacientes. “É um avanço gigantesco para a oncologia nacional. Essa medicação pode reduzir em até 50% a mortalidade das pacientes com esse tipo de câncer. É uma grande vitória para a saúde pública e para o povo brasileiro”, destacou José Barreto, diretor do Departamento de Atenção ao Câncer do Ministério da Saúde.
O investimento total é de R$ 159,3 milhões para a aquisição de 34,4 mil frascos-ampola, e o governo federal ainda negocia valores cerca de 50% abaixo do mercado, o que pode gerar economia de R$ 165,8 milhões e ampliar o acesso ao tratamento.
Segundo o Ministério da Saúde, estão previstos quatro lotes do medicamento, com novas entregas programadas para dezembro de 2025, março e junho de 2026, atendendo 100% da demanda atual e beneficiando 1.144 pacientes em 2025.
Outras notícias sobre saúde e avanços no tratamento de doenças você confere no Ilhéus Eventos.
Acesse www.ilheuseventos.com.br e siga a gente no Instagram @ilheuseventos.


Sorry, the comment form is closed at this time.